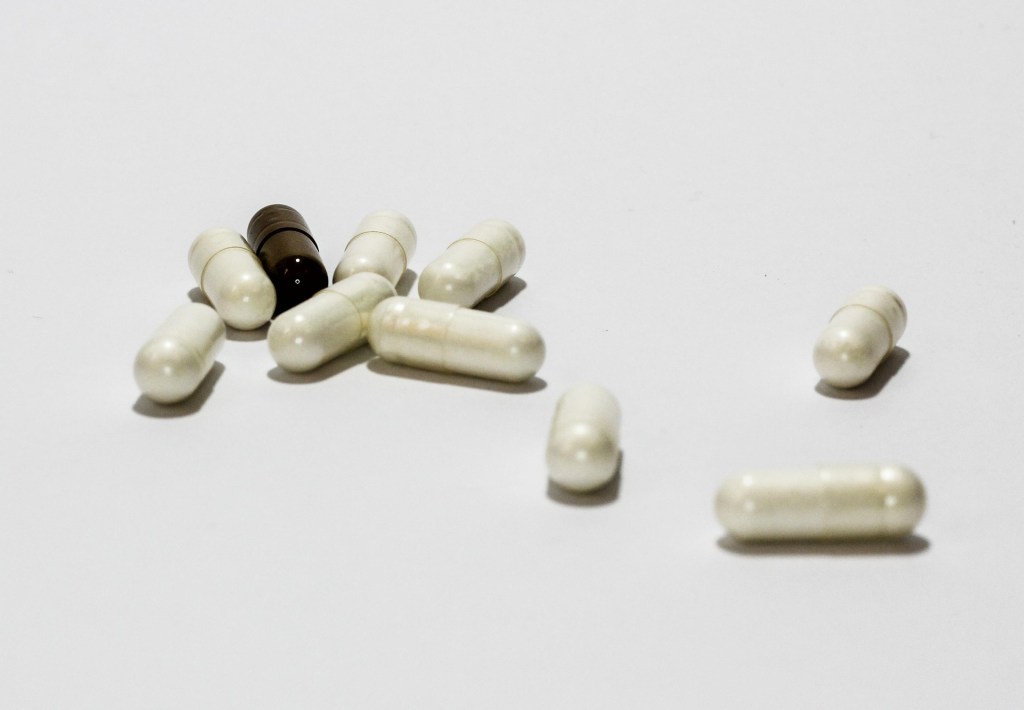
Gli antibiotici, farmaci indispensabili per combattere infezioni batteriche anche gravi, possono alterare l’equilibrio del microbiota intestinale per periodi molto più lunghi di quanto si ritenesse finora. In alcuni casi basta un singolo ciclo di terapia per lasciare segni rilevabili anche quattro-otto anni dopo l’assunzione.
Il dato emerge da uno studio scientifico realizzato in Svezia e pubblicato sulla rivista internazionale Nature Medicine. I ricercatori hanno analizzato la relazione tra la storia terapeutica di quasi 15mila adulti e la composizione del loro microbiota intestinale, osservando effetti persistenti associati ad alcune classi di antibiotici.
Il lavoro approfondisce il cosiddetto effetto collaterale “indiretto” di questi farmaci: mentre eliminano i batteri responsabili delle infezioni, possono colpire anche quelli utili che vivono nell’intestino umano.
Cos’è il microbiota intestinale e perché è importante
Con il termine microbiota intestinale si indica l’insieme di batteri, virus e altri microrganismi che abitano l’apparato digerente. Questa comunità biologica svolge funzioni fondamentali: contribuisce alla digestione, partecipa alla regolazione del sistema immunitario e influisce su diversi processi metabolici.
Gli effetti immediati degli antibiotici su questo ecosistema sono noti da tempo. Le terapie antimicrobiche possono ridurre la varietà delle specie batteriche presenti nell’intestino e modificarne la composizione.
Quello che finora non era stato chiarito con precisione era quanto a lungo potessero persistere queste alterazioni.
Il nuovo studio coordinato da ricercatori dell’Università di Uppsala affronta proprio questo punto, collegando i dati sulle prescrizioni farmacologiche con le analisi genetiche del microbiota intestinale.
Secondo Gabriel Baldanzi, primo autore dello studio ed ex dottorando dell’ateneo svedese:
“Possiamo osservare che l’uso di antibiotici risalente a 4-8 anni prima è correlato alla composizione del microbiota intestinale di una persona oggi. Anche un singolo ciclo di trattamento con alcuni tipi di antibiotici lascia tracce”.
Il possibile legame con alcune malattie
Diversi studi epidemiologici pubblicati negli ultimi anni hanno evidenziato un’associazione tra uso frequente di antibiotici e aumento del rischio di alcune patologie.
Tra queste sono state osservate correlazioni con:
- diabete di tipo 2;
- infezioni gastrointestinali.
Gli scienziati sottolineano però che i meccanismi biologici alla base di questa relazione non sono ancora completamente chiariti.
Una delle ipotesi più accreditate riguarda proprio le modifiche del microbiota intestinale. Cambiamenti persistenti nella comunità microbica potrebbero infatti influenzare processi metabolici e immunitari.
Il nuovo studio fornisce, quindi, un ulteriore tassello per comprendere il possibile ruolo delle terapie antibiotiche nel lungo periodo.
La ricerca su 14.979 adulti in Svezia
Per analizzare il fenomeno, i ricercatori hanno esaminato i dati relativi a 14.979 adulti residenti in Svezia.
Il lavoro è stato reso possibile dall’integrazione di due importanti fonti di informazioni:
- il registro nazionale svedese dei farmaci da prescrizione;
- le biobanche universitarie di Uppsala e Lund, che contengono dati sul microbiota intestinale.
Il registro dei farmaci raccoglie informazioni su tutti gli antibiotici dispensati nelle farmacie svedesi, consentendo di ricostruire con precisione le terapie ricevute dai partecipanti.
Questi dati sono stati messi in relazione con le analisi genetiche del microbiota intestinale presenti nelle biobanche universitarie.
In questo modo gli scienziati hanno potuto confrontare la composizione microbica tra:
- persone che avevano assunto antibiotici;
- persone che non avevano ricevuto trattamenti nello stesso periodo.
Dallo studio emerge, inoltre, che l’impatto sul microbiota non è uguale per tutti gli antibiotici.
Le alterazioni più marcate sono state associate a:
- clindamicina;
- fluorochinoloni;
- flucloxacillina.
La penicillina V, invece, antibiotico molto utilizzato in Svezia per le infezioni trattate fuori dall’ospedale, risulta collegata a cambiamenti più contenuti e temporanei.
Il risultato inatteso sulla flucloxacillina
Tra i risultati della ricerca, uno ha attirato particolare attenzione. Riguarda la flucloxacillina, antibiotico a spettro relativamente ristretto.
Come osserva Tove Fall, professoressa di epidemiologia molecolare all’Università di Uppsala e responsabile dello studio:
“Il forte legame tra la flucloxacillina a spettro ristretto e il microbiota intestinale è stato inaspettato e vorremmo vedere questa scoperta confermata in altri studi”.
Secondo la ricercatrice, le conclusioni del lavoro potrebbero contribuire a orientare le decisioni terapeutiche future:
“Tuttavia, crediamo che i risultati del nostro studio possano contribuire a orientare le future raccomandazioni sull’uso degli antibiotici, soprattutto quando si sceglie tra due antibiotici ugualmente efficaci, uno dei quali ha un impatto più debole sul microbiota intestinale”.
I limiti dello studio e i prossimi passi
Gli autori segnalano alcuni limiti metodologici della ricerca.
L’analisi ha preso in considerazione solo le prescrizioni antibiotiche degli ultimi otto anni. Periodi di osservazione più lunghi potrebbero fornire ulteriori informazioni sugli effetti a lungo termine.
Inoltre, per ogni partecipante è stato raccolto un solo campione di microbiota intestinale.
Per migliorare la comprensione del fenomeno, il team di ricerca ha avviato una nuova fase dello studio.
Come spiega ancora Tove Fall:
“Stiamo attualmente raccogliendo un secondo campione da quasi la metà dei partecipanti. Questo ci permetterà di comprendere ancora meglio i tempi di recupero e di identificare quali microbiota intestinali sono più suscettibili ad alterazioni dopo il trattamento antibiotico”.






Commenta con Facebook