Un nuovo farmaco sperimentale per il tumore al pancreas ha portato la sopravvivenza mediana da 6,7 a 13,2 mesi in uno studio clinico di Fase 3. Il dato, comunicato da Revolution Medicines, riguarda pazienti il cui tumore era già progredito dopo altre terapie. L’impatto è diretto: +6,5 mesi di vita e rischio di morte ridotto del 60% rispetto alla chemioterapia standard.
Il farmaco, chiamato daraxonrasib, è una compressa giornaliera che ha centrato tutti gli endpoint principali e secondari dello studio.
“Questi sono risultati drammatici, destinati a cambiare la pratica clinica, e ora il nostro obiettivo è portare rapidamente questa opzione ai pazienti che ne hanno urgente bisogno”, ha dichiarato l’amministratore delegato Mark Goldsmith.
Come funziona daraxonrasib e perché è diverso
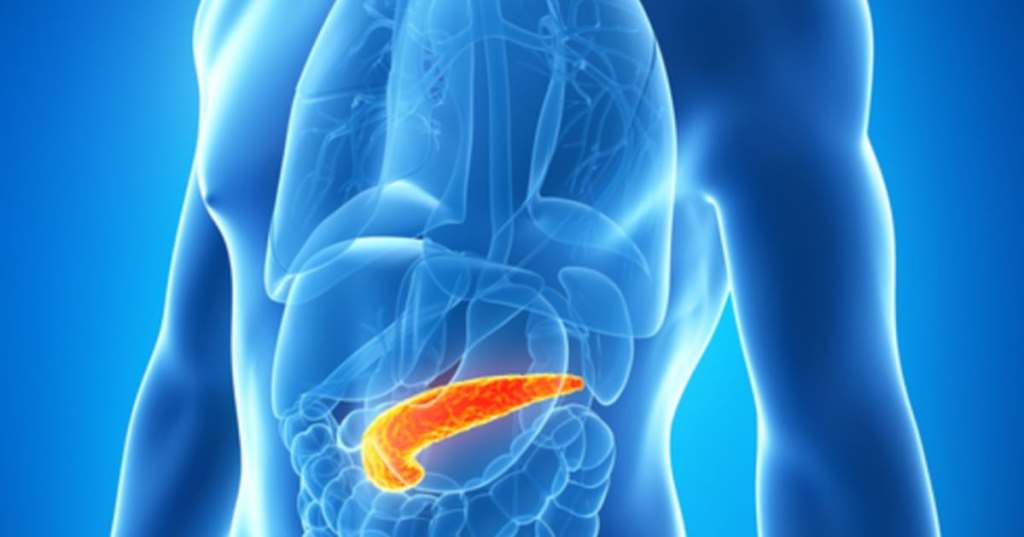
Il tumore al pancreas è tra i più aggressivi: il tasso di sopravvivenza a cinque anni si ferma al 13%. Una delle ragioni è la presenza, in circa il 90% dei casi, di mutazioni del gene RAS, che alimentano la crescita tumorale.
Daraxonrasib agisce proprio su questo bersaglio. Finora, i pazienti venivano trattati quasi esclusivamente con chemioterapia endovenosa citotossica. Il nuovo approccio è mirato e orale.
Il dr. Goldsmith ha definito i risultati “senza precedenti”, sottolineando che nessun farmaco aveva mai superato un anno di sopravvivenza in uno studio di Fase 3 per questo tumore.
Iter regolatorio: richiesta accelerata negli Stati Uniti
L’azienda ha annunciato che presenterà a breve la domanda di approvazione alla Food and Drug Administration utilizzando un “Commissioner’s National Priority Voucher”, che consente una revisione in pochi mesi.
L’indicazione iniziale sarà per pazienti già trattati (seconda linea), mentre è in corso un altro studio di Fase 3 su pazienti appena diagnosticati.
Le reazioni dei medici: “risultati trasformativi”
Secondo il professor Shubham Pant, oncologo del The University of Texas MD Anderson Cancer Center, i dati rappresentano una svolta reale: “Per i pazienti questi risultati sono davvero trasformativi”.
Pant ha partecipato allo sviluppo del farmaco fin dalle fasi iniziali. Durante le dichiarazioni, ha mostrato forte coinvolgimento emotivo parlando dei pazienti seguiti: “Oggi posso solo dire che sono grato. Vedere i pazienti in ambulatorio, anche oggi, mi fa dire solo questo: sono grato”.
Il caso Ben Sasse: riduzione del tumore del 76%
Il farmaco ha attirato attenzione mediatica dopo il racconto dell’ex senatore statunitense Ben Sasse in un’intervista al The New York Times.
Diagnosi a fine 2025 e prognosi di pochi mesi, Sasse ha riferito una riduzione del 76% delle masse tumorali dopo l’inizio della terapia.
Ha però descritto effetti collaterali significativi: “come un’eruzione cutanea sul viso”. Durante l’intervista, il volto appariva irritato e desquamato.
Effetti collaterali e gestione clinica
Secondo i dati disponibili:
- La maggioranza dei pazienti sviluppa rash cutaneo;
- Meno del 10% presenta forme gravi;
- Possibili interventi: sospensione temporanea o antibiotici.
Pant ha spiegato che la gestione degli effetti collaterali sta migliorando nel tempo: “Negli ultimi tre anni stiamo diventando sempre più capaci di gestire questi effetti”.
L’azienda ha dichiarato che il profilo di sicurezza è gestibile e che non sono emerse nuove criticità nello studio principale.
Impatto clinico: una base per nuove terapie combinate
Per Andrew Aguirre del Dana-Farber Cancer Institute, il risultato rappresenta una base su cui costruire nuove combinazioni terapeutiche.
Ha definito il miglioramento “enorme” e ha aggiunto: “È un motivo di ottimismo per tutto il settore. Colpire RAS in questi pazienti, e in altri contesti difficili, può portare benefici concreti”.
Effetti sul mercato e valore aziendale
Dopo l’annuncio, il titolo di Revolution Medicines è salito di oltre il 30% in un giorno.
- Crescita annuale: +274%;
- Valore di mercato: oltre 26 miliardi di dollari.
Nonostante le speculazioni su possibili acquisizioni, l’azienda ha ribadito che la priorità resta l’approvazione e il lancio del farmaco.
Per l’Italia, infine, il percorso non sarebbe immediato. Dopo l’eventuale autorizzazione FDA, servirebbero il passaggio europeo e poi i tempi nazionali di accesso e rimborsabilità.
⚠️ Disclaimer
Le informazioni contenute in questo articolo hanno finalità esclusivamente informative e giornalistiche. Non sostituiscono in alcun modo il parere del medico, dell’oncologo o di altri professionisti sanitari qualificati. I dati riportati derivano da studi clinici, fonti istituzionali e comunicazioni ufficiali, ma riguardano risultati sperimentali che potrebbero non essere ancora disponibili nella pratica clinica o autorizzati in Italia. Ogni decisione relativa a diagnosi, terapia o utilizzo di farmaci deve essere presa insieme al proprio medico curante o allo specialista di riferimento, sulla base della situazione clinica individuale. L’autore e la redazione non sono responsabili per eventuali usi impropri delle informazioni presenti nel testo.






Commenta con Facebook