In Europa aumentano ogni giorno i nuovi casi di Covid-19 e l’Agenzia Europea del Farmaco (EMA) “fornirà raccomandazioni a livello UE nel più breve tempo possibile per aiutare le autorità nazionali a decidere sul possibile uso precoce” del medicinale anti Covid-19 per via orale molnupiravir prodotto dalla Merck “ad esempio, in contesti di emergenza”.
Lo ha reso noto l’EMA, precisando che la strategia è stata concordata insieme ai capi delle agenzie per i medicinali nazionali. Per EMA e autorità nazionali, secondo quanto si legge in una nota, sono necessari “ulteriori orientamenti sui trattamenti per il COVID-19 alla luce dell’aumento dei tassi di infezione e dei decessi”.
L’EMA sta riesaminando i dati disponibili sull’uso del medicinale anti Covid-19 “per sostenere le autorità nazionali che potrebbero decidere sull’uso di questo farmaco per il trattamento del Covid-19 prima della sua autorizzazione”.
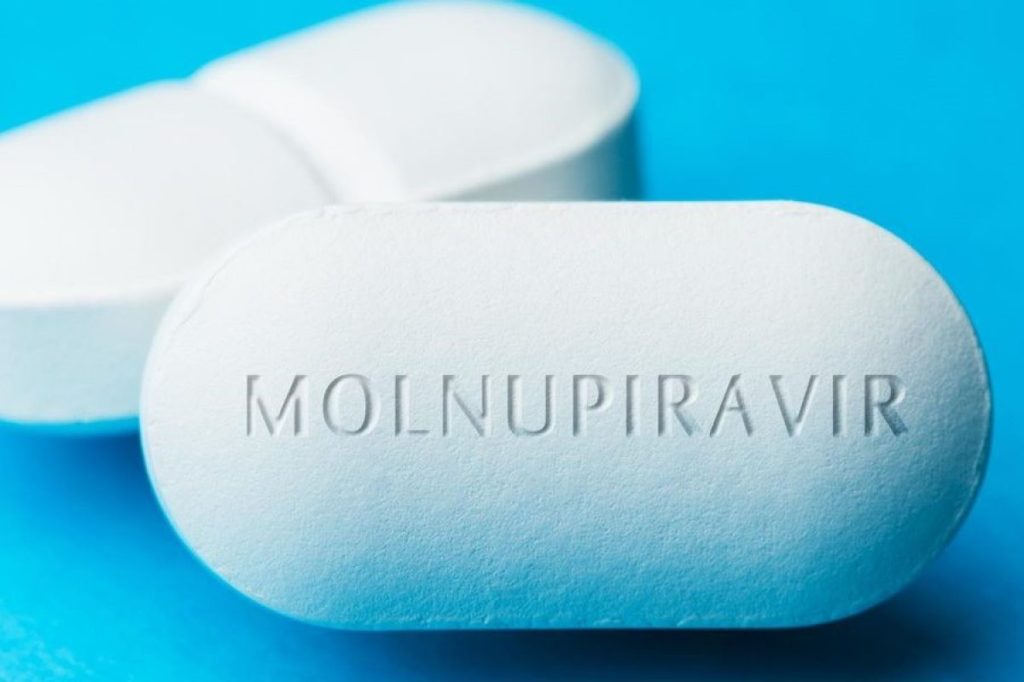
Il molnupiravir è un medicinale antivirale orale sviluppato da Merck Sharp & Dohme in collaborazione con Ridgeback Biotherapeutics, ed è già stato autorizzato nel Regno Unito. Il servizio sanitario nazionale britannico, infatti, inizierà uno studio clinico della pillola anti-Covid della Merck entro la fine del mese: lo ha reso noto Susan Hopkins, Chief Medical Adviser dell’Agenzia per la sicurezza sanitaria britannico. Il governo di Londra ha acquistato 480mila dosi del farmaco antivirale, oltre a 250mila dosi della pillole antivirali sviluppate dalla Pfizer per la cui autorizzazione dovrebbero trascorrere altri due mesi, secondo quanto spiegato da Hopkins alla BBC.






Commenta con Facebook